胰腺癌新药,NRG1基因突变靶向药MCLA-128(Zenorcutuzumab)使晚期胰腺癌患者有救了
胰腺癌是一种恶性程度非常高的恶性肿瘤,一直以来都位居“癌中之王”的地位,就是因为其恶性程度高、治疗效果差、生存时间短、死亡率高。胰腺癌患者1年生存期约为20%,5年生存期约为3%。在过去20年中,其总体的手术切除率、1年生存率和5年生存率无显著变化。
尽管手术仍然是胰腺癌首要的治疗方法,但是,由于胰腺癌常常发现较晚,极易丧失根治的机会。因此,对胰腺癌的治疗亟需新的治疗方法。
MCLA-128的面世,晚期胰腺癌有救了
近年来,随着分子靶向治疗的迅猛发展,胰腺癌的治疗获得了众多的突破。2020年,美国(FDA)授予MCLA-128(zenorcutuzumab)孤儿药地位,用于NRG1融合突变胰腺癌的治疗。
MCLA-128是一款针对HER2、HER3双靶点的新型抗癌靶向药。可与HER2和HER3受体结合,从而阻断HER3及其配体神经调节蛋白1(NRG1)或NRG1融合蛋白的相互作用,对于NRG1基因融合的胰腺癌患者效果显著。
2020年2月,Merus公布了双特异性抗体MCLA-128在治疗携带NRG1融合突变胰腺癌中的初步临床结果。
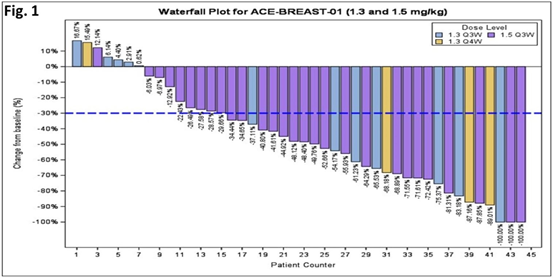
试验结果表明,MCLA-128在这2名胰腺癌患者中都让肿瘤体积出现缩小。
第一位胰腺癌患者:8周时的影像显示肿瘤直径缩小44%,在随后的5个月确认性扫描中进一步改善为缩小54%。正电子发射断层扫描显示没有代谢活跃肿瘤的迹象,相关的血清生物标记物(CA19-9)显示在最初4周内表现改善。而且,在第一次给药后的几周内,患者的症状包括疲劳和体重减轻,都有所改善。经过7个多月的治疗,患者仍在接受治疗。
第二位胰腺癌患者:7周时的影像显示肿瘤直径缩小22%,5个月后的确认性扫描显示肿瘤直径缩小25%;PET影像显示没有代谢活跃肿瘤的迹象。患者因肿瘤引起的腹痛在治疗后得到改善。经过7个多月的治疗,患者仍在接受治疗。
毫无疑问,MCLA-128作为首款正式获得FDA批准的广谱抗癌药靶向药,用于治疗NRG1突变的胰腺癌患者,具有重要里程碑的意义。
另外,在安全性方面,MCLA-128在1/2期临床试验中仍具有良好的耐受性,117例接受单药MCLA-128治疗的患者,每周至每三周一次的给药方案,报告的不良事件大多为轻度至中度(AE)。3级和4级不良事件的发生率分别为37%和3%,疑似药物相关3级不良事件的发生率约为4%,无疑似药物相关4级事件。一名患者出现5级过敏反应。
胰腺癌新靶标NRG1,为患者带来全新希望
NRG1(神经调节蛋白1)融合突变是一个罕见的致癌驱动基因,在多种实体瘤中均被发现,如非小细胞肺癌、胆囊癌、胰腺癌、肾癌、卵巢癌、膀胱癌、结直肠癌及肉瘤等多种常见实体瘤中检出,但整体发生率极低。如在非小细胞肺癌中的发生率仅有0.3%,在胰腺导管腺癌中的发生率也仅有0.5%至1.5%,但在特殊病理类型肺粘液腺癌则达到7-31%。
在最新发布的胰腺癌NCCN指南中明确建议:胰腺癌患者除了检测KRAS、CDKN2A、TP53和SMAD4这四个最为常见的突变,近年来,一些研究的热点基因,包括NRG1,NTRK,BRCA1,BRCA2等基因进行检测,可以帮助确定更有效的治疗方法,以及是否有机会参与新药的临床研究。
大家可以致电全球肿瘤医生网医学部(4006667998)咨询具体需要检测的基因靶点,
做过基因检测的患者,可将检测报告,如基因检测报告,诊断报告以电子版或拍照发送至doctor.huang@globecancer.com,我们将为您分析报告,匹配是否有新药使用。请在邮件中留下联系方式,全球肿瘤医生网医学部收到报告分析完毕后,会在一个工作日内电话联系您。