5月18日,阿斯利康/第一三共联合宣布FDA授予其Enhertu(trastuzumabderuxtecan)第3个突破性疗法认定,用于治疗铂类化疗后疾病进展的HER2突变、转移性非小细胞肺癌(NSCLC)患者。
肺癌是全球癌症死亡的主要原因。据估计,2020年全球新确诊肺癌病例将超过220万例,美国将超过22万例,大约超过13万例患者会因此死亡。NSCLC患者大约占肺癌患者的85%,其中,大约有2-4%的NSCLC患者发生了HER2突变。转移性肺癌患者预后很差,5年生存率大约为6-10%。目前,尚无针对HER2mNSCLC患者的药物获批。
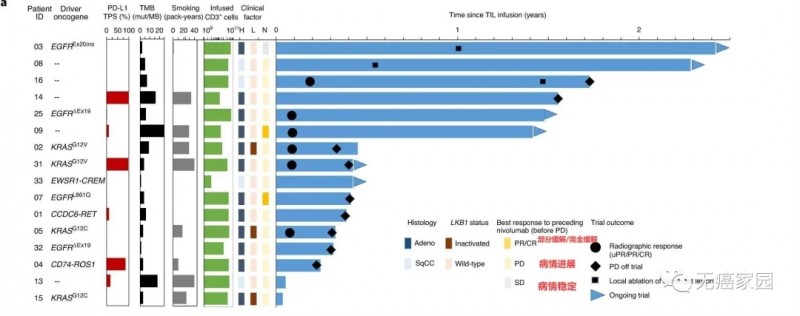
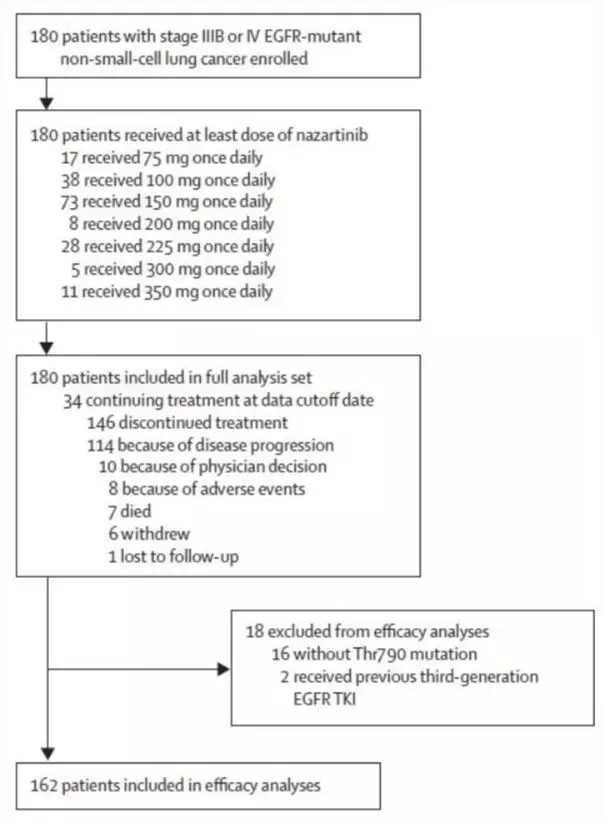
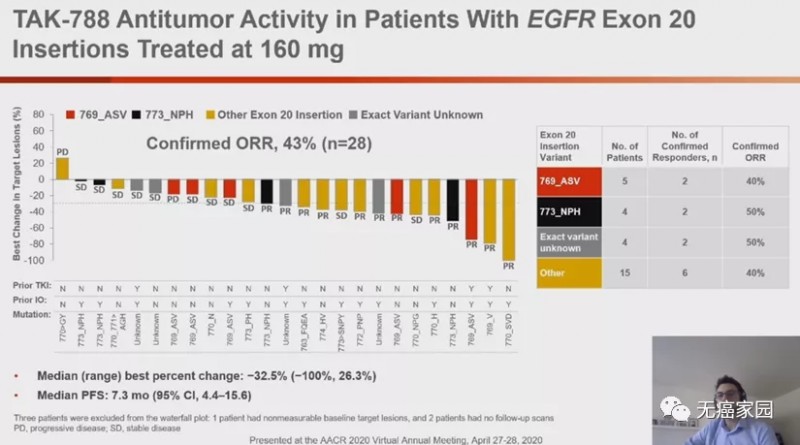
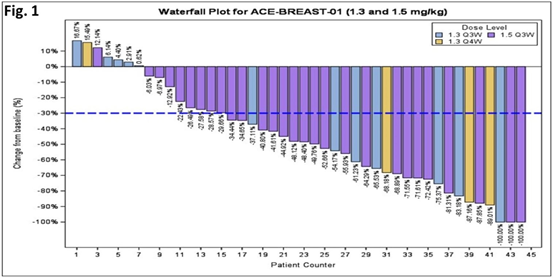
此次突破性疗法认定是基于II期DESTINY-Lung01研究数据。该研究共纳入90例HER2m患者和80例HER2过度表达患者。该研究的中期分析详细数据将于即将进行的ASCO20会议上公布。目前,已经公布的摘要数据显示,中位随访8个月,接受Enhertu治疗的患者ORR为61.8%,中位应答持续时间尚未到达,26例产生应答的患者中有16例正在接受治疗,DCR为90.5%,估计中位PFS为14.0个月。
安全性方面,最常见的不良事件是胃肠道和血液系统疾病,包括恶心、脱发、贫血、食欲下降和中性粒细胞减少。HER2mNSCLC患者中有5例发生药物相关的间质性肺病和肺炎,均为2级。
厦大原创抗癌新药获美FDA临床试验许可
厦大日前对外发布消息称,厦大药学院院长张晓坤教授领导团队研发的原创抗癌新药,已经获得美国FDA的临床试验许可批件,正式进入新药在被批准上市前必经的临床试验阶段,将开展在晚期结直肠癌患者中的临床测试。研究者在对结直肠癌、胃癌及乳腺癌患者肿瘤组织进行临床样品检测时发现,他们的肿瘤组织中含有大量的tRXRα癌蛋白,也就是说,这类患者体内有足够多的K-80003药物作用的起效对象,用药治疗的成效将十分显著。该原创抗癌新药K-80003源于张晓坤教授2010年在厦大做出的重要学术发现,它是一种靶向结肠癌等癌症的高表
0评论2025-12-0810
7月FDA大事记:免疫治疗适应症再次拓展,多款“老药”焕发新光彩
日期:2021年7月22日状态:批准(加速批准转为正式批准)相关阅读:暂无相关临床试验及数据:【KEYNOTE-775/Study309试验】派姆单抗+乐伐替尼治疗的中位总生存期为17.4个月,中位无进展生存期6.6个月,整体缓解率30%。相关临床试验及数据:【SANET-p试验/胰腺神经内分泌肿瘤】受索凡替尼治疗的患者,整体缓解率为19.2%,中位无进展生存期为10.9个月。适应症:单药治疗无法通过手术或放疗治愈的局部晚期皮肤鳞状细胞癌日期:2021年7月6日状态:补充适应症相关阅读:暂无相关临床试验及
0评论2025-12-0619