今日,美国FDA宣布批准阿斯利康的Lynparza片剂,用于复发性上皮卵巢癌、输卵管癌、或原发性腹膜癌成人患者的维持治疗。这些患者在先前接受铂类化疗后,正处于完全或部分缓解期。
卵巢癌是女性癌症患者最常见的死因之一。在带有BRCA突变等特定遗传性基因异常的情况下,女性发生卵巢癌的风险会显著增加。由阿斯利康研发的olaparib是一款口服聚ADP核糖聚合酶抑制剂,可以利用肿瘤DNA损伤反应通路缺陷来杀伤癌细胞。2014年,olaparib胶囊获得了美国FDA的加速批准,治疗带有BRCA基因突变的晚期卵巢癌患者。
在两项随机、设置安慰剂对照的双盲、多中心临床试验中,研究人员进一步评估了这款药物作为维持疗法的可行性。在第一项名为SOLO-2的临床试验里,研究人员招募了295名复发性卵巢癌、输卵管癌、或是原发性腹膜癌患者,她们都带有gBRCA突变,且正处于铂类化疗后的缓解期。研究发现,接受olaparib治疗的患者,无进展生存期为19.1个月,相较对照组的患者得到了显著延长。
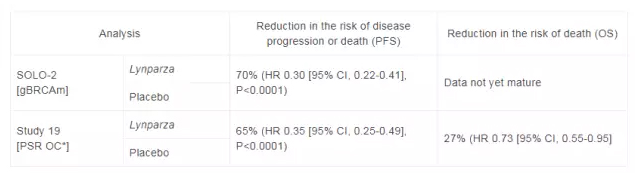
FDA的批准基于这两项试验的成功
在另一项代码为NCT00753545的临床试验里,研究人员招募了265名患者,她们的BRCA突变状况未纳入考量。研究发现,服用olaparib的患者,中位PFS为8.4个月,也显著超过了对照组。基于这两项试验结果,美国FDA批准了olaparib的片剂,作为这些适应症的维持疗法。值得注意的是,olaparib片剂与olaparib胶囊并不能通用。

阿斯利康全球医药开发执行副总裁兼首席医学官SeanBohen博士
“医生们在Lynparza的使用上已经有了快3年的经验。今天我们很高兴带来这一重要药物的新制剂形式,造福更广大的妇女群体,”阿斯利康全球医药开发执行副总裁兼首席医学官SeanBohen博士说道:“今日的批准验证了Lynparza背后10多年的辛勤研究。这款全球首个PARP抑制剂能让肿瘤学家在治疗选择上有更大的灵活性。基于最近与默沙东的合作,我们将进一步为患者带来更多治疗方案。”
参考资料
[1]LynparzareceivesadditionalandbroadapprovalintheUSforovariancancer
[2]FDAapprovesolaparibtabletsformaintenancetreatmentinovariancancer