KRASG12C抑制剂,癌症肿瘤中KRASG12C抑制剂的获得性耐药机制
尽管许多接受KRASG12C抑制剂治疗的癌症患者观察到了临床获益,但大多数患者最终还是出现了对单药治疗的获得性耐药,KRASG12C抑制剂临床获得性耐药的潜在机制是什么呢?
⑴我们每个人的体内都有一种叫做KRAS的蛋白质。蛋白质是人体细胞、组织和器官的结构和功能所必须的;1
⑵KRAS蛋白的工作原理就像一个开关,传递信息,告诉细胞何时生长,何时停止生长;2
⑶有时蛋白质会发生突变(改变)并产生异常的功能,KRASG12C是KRAS蛋白的一种突变;2
⑷KRASG12C突变会使开关卡在“开”的位置,导致细胞持续不可控的生长,从而形成肿瘤;3
⑸NSCLC中,最常见的生物标志物之一是KRASG12C;4
⑹在美国,每8名NSCLC患者中就有1名是KRASG12C;在中国,每33名NSCLC患者中就有1名是KRASG12C;4,5
⑺知道是否有KRASG12C生物标志物的唯一方法是基因检测,组织活检或液体活检均可;6
⑻如果检测到KRASG12C生物标志物,这意味着可以选择KRASG12C抑制剂的靶向治疗方案;7
⑼KRASG12C抑制剂会出现获得性耐药吗?临床耐药机制是什么呢?8
KRAS是癌症中最常见的突变致癌基因之一
KRAS蛋白是一种鸟苷三磷酸酶(GTPase),它受到细胞外的刺激时,可在激活的鸟苷三磷酸(GTP)结合状态和失活的鸟苷二磷酸(GDP)结合状态之间循环,以此发挥分子开关的作用。
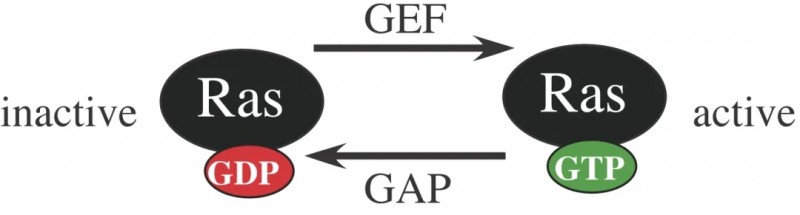
KRAS中的致癌突变通常发生在KRAS蛋白的热点位置(例如,密码子12、13和61),该突变有利于KRAS的活性形式(突变后的KRAS影响其与GAP蛋白的结合能力,从而抑制GAP诱导的GTP水解),导致与GTP结合的KRAS浓度异常增高,进而激活下游的MAPK和PI3K等通路驱动肿瘤的发生与发展。
由于KRAS和GTP的结合亲和力在皮摩尔级,GTP的细胞内浓度又很高,而且与GTP结合的KRAS蛋白缺乏结合口袋,因此直接抑制结合GTP,处于激活状态的KRAS蛋白是非常困难的。9这也是近40年来,大家认为KRAS突变是“不可成药”靶点的原因。
然而,随着KRAS蛋白机制和结构的新见解,大家发现,当KRASG12C蛋白和GDP结合,处于失活状态的KRASG12C蛋白中,存在着一个能够被共价抑制剂结合的位点,如果这时候开发出一款靶向药,将KRAS蛋白锁定在失活状态,便可以抑制KRASG12C突变蛋白的活性(而不影响未突变KRAS蛋白的正常功能),进而阻断依赖该蛋白的致癌信号通路。9基于这种思路,KRASG12C这一“不可成药”靶点有了重大突破,受到了业界的广泛关注。
KRASG12C抑制剂已经吸引了制药企业的大量投资和兴趣,其中两个比较出名的KRASG12C抑制剂为sotorasib(AMG510;2021年5月28日,FDA批准sotorasib用于KRASG12C突变NSCLC患者10)和adagrasib(MRTX849;2021年6月24日,FDA授予adagrasib用于KRASG12C突变NSCLC患者的突破性疗法认定11)。
KRASG12C抑制剂的耐药机制
尽管许多接受KRASG12C抑制剂治疗的癌症患者观察到了临床获益,但大多数患者最终还是出现了对单药治疗的获得性耐药,目前对KRASG12C抑制剂耐药的临床机制知之甚少。
2021年6月24日,发表于《新英格兰医学杂志》的一项研究,对癌症中KRASG12C抑制剂的获得性耐药机制进行了详细的描述,包括在靶耐药:KRASG12C突变以外的其他KRAS突变(例如G12D,G13D和Y96C等)或KRASG12C扩增;脱靶耐药:KRAS以外的其他基因变异,包括NRAS、BRAF、MET、ALK和RET等;组织学转化(例如从腺癌转化为鳞癌)。8此次发现,有助于开发更好的KRAS抑制剂和新的组合疗法来延迟或克服KRASG12C突变癌症的耐药性。

此研究共纳入38名接受adagrasib单药治疗时出现疾病进展的KRASG12C突变癌症患者,其中27名为非小细胞肺癌,10名为结直肠癌和1名为阑尾癌。
耐药机制从以下两个角度进行分析:
1)组织学角度:对adagrasib获得性耐药时取得的组织活检样本的组织学特征与adagrasib治疗前获得的组织学特征进行比较;
2)分子生物学角度:对adagrasib获得性耐药时取得的组织活检样本或血浆ctDNA进行NGS检测,并将结果与adagrasib治疗前可用的组织或血浆ctDNA测序结果进行比较。
研究结果发现,在38名癌症患者中,有17名(45%)确定了adagrasib的潜在耐药机制,其中7名(18%)存在多重耐药机制。换句话说就是,在45%的癌症患者中确定了KRASG12C抑制剂的潜在耐药机制,59%(10/17)为单一耐药机制,41%(7/17)多重耐药机制。
总的来说,KRASG12C抑制剂的获得性耐药机制可分为三大类:
1)KRASG12C抑制剂在靶耐药(on-target):
获得性KRAS突变包括G12D/R/V/W、G13D、Q61H、R68S、H95D/Q/R、Y96C或KRASG12C扩增;
2)KRASG12C抑制剂脱靶耐药(off-target):
获得性旁路耐药机制包括MET扩增,NRAS、BRAF、MAP2K1和RET的激活突变,ALK、RET、BRAF、RAF1和FGFR3的致癌融合,以及NF1和PTEN中的功能缺失突变;
3)组织学转化:
在可获得配对组织活检样本的9名肺腺癌患者中,有2名观察到组织学转化为鳞状细胞癌。
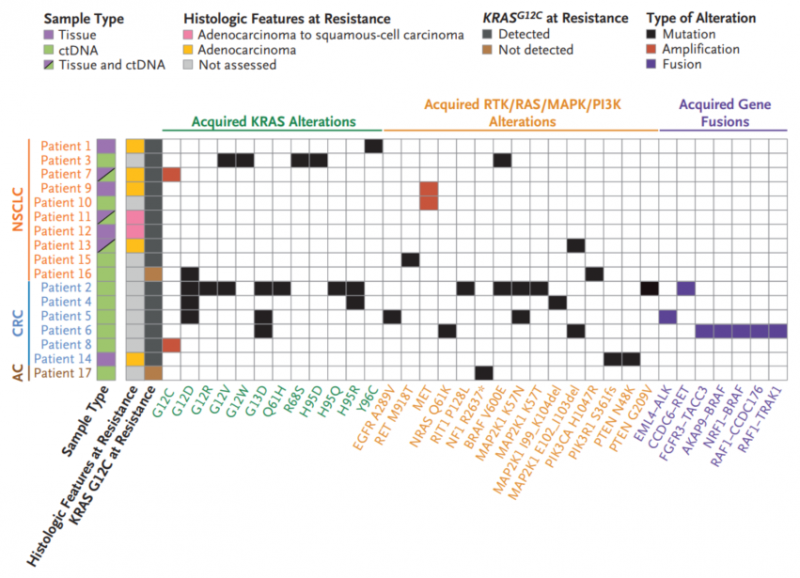
▲adagrasib的获得性耐药机制总结
另外需要注意的是,该研究侧重于接受adagrasib治疗患者的获得性耐药机制,并未评估接受sotorasib治疗的患者,因此,sotorasib的获得性耐药机制目前尚不清楚,临床不能直接比较adagrasib和sotorasib的耐药机制。
adagrasib和sotorasib之间不同的药物结合机制可导致药物特异性耐药突变的出现。比如,Y96C突变对这两种抑制剂都表现出高水平耐药性,而H95D/Q/R突变对adagrasib产生耐药性,而对sotorasib没有产生耐药性,这与分子结构略有不同的ALK抑制剂其实非常像。
当然,目前还没有任何临床病例可以证明KRASG12C患者可以从一种KRASG12C抑制剂转向另一种,研究人员虽然发现这一现象,但进一步研究依然很重要。
此外,研究人员使用体外深度突变扫描(大规模并行测序在单个实验中同时测量蛋白质中许多变体的功能影响的方法),系统地揭示了KRASG12C抑制剂(adagrasib和sotorasib)的获得性耐药突变全貌,为KRASG12C抑制剂的耐药机制提供了参考。
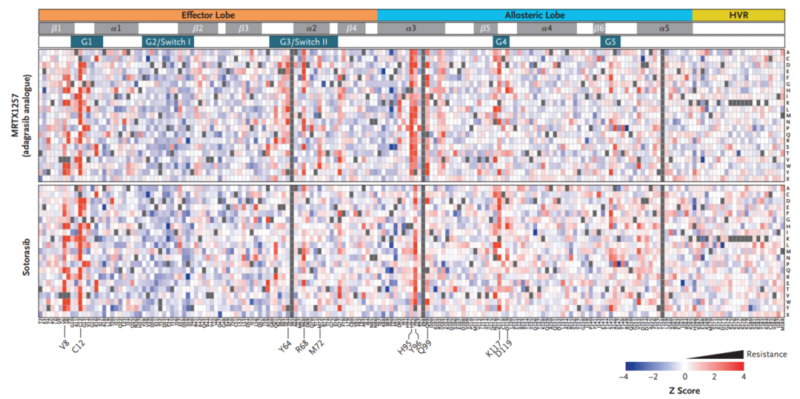
▲深度突变扫描揭示KRASG12C抑制剂的耐药突变情况
总的来说,这些数据表明,KRASG12C抑制剂存在多种在靶和脱靶耐药机制,有助于开发更好的KRAS抑制剂和新的组合疗法(包括PD-1/L1,SHP2,Pan-EGFR,CDK4/6和SOS1抑制剂等)来延迟或克服KRASG12C突变癌症的耐药性。
KRASG12C抑制剂虽然有耐药的情况出现,但是对患者还是很有意义的,也有免费的临床试验可以参加,有想要进一步了解的读者可以在线咨询客服。
参考资料:
1.NCIDictionaryofCancerTerms.NIHNationalCancerInstitutewebsite.https://www.cancer.gov/publications/dictionaries/cancer-terms/.AccessedDecember16,2020.
2.RyanMB,CorcoranRB.NatRevClinOncol.Vol15.2018.
3.HongDS,FakihMG,StricklerJH,etal.NEnglJMed.2020.
4.Dataonfile,Amgen;[AnalysisofAACRGeniev8].
5.LiuSi-Yang,SunHao,ZhouJia-Yingetal.KRASG12CClinicalcharacteristicsandprognosticvalueofthemutationinChinesenon-smallcelllungcancerpatients.[J].BiomarkRes,2020,8:22.
6.KalemkerianGP,NarulaN.KennedyEB,etal.JClinOncol.Vol36.2018.
7.LUMAKRAS™(sotorasib)PatientInformation.ThousandOaks,CA:Amgen;2021.
8.AwadMarkM,LiuShengwu,RybkinIgorIetal.AcquiredResistancetoKRASG12CInhibitioninCancer.[J].NEnglJMed,2021,384:2382-2393.
9.SkoulidisFerdinandos,LiBobT,DyGraceKetal.SotorasibforLungCancerswithKRASp.G12CMutation.[J].NEnglJMed,2021,384:2371-2381.
10.https://www.fda.gov/drugs/drug-approvals-and-databases/fda-grants-accelerated-approval-sotorasib-kras-g12c-mutated-nsclc
11.https://ir.mirati.com/press-releases/press-release-details/2021/Mirati-Therapeutics-Adagrasib-Receives-Breakthrough-Therapy-Designation-from-U.S.-Food-and-Drug-Administration-for-Patients-with-Advanced-Non-Small-Cell-Lung-Cancer-Harboring-the-KRAS-G12C-Mutation/default.aspx
