免疫治疗需要做基因检测吗,哪些癌症肿瘤患者适合用免疫治疗(PD-1)抑制剂
问世之初,PD-1抑制剂曾经以出色的疗效以及更少的副作用,成为了无数癌症患者心目中的“神药”。而如今,越来越多的药企加入了PD-1/PD-L1抑制剂的研发行列之中。
新药的研发步伐加快,自然也就有了越来越多的上市PD-1抑制剂,以及PD-1抑制剂的临床试验。免疫治疗越来越普及,更多患者有了使用“神药”的机会。
今天,基因药物汇带大家一起来了解一下,用PD-1抑制剂之前需要做基因检测吗?哪些基因突变,会对PD-1抑制剂的疗效造成影响?哪些患者更适合使用PD-1抑制剂治疗?
这些检测,对PD-1抑制剂方案的选择最为关键
目前,已经获得FDA批准,用于规范PD-1抑制剂的适应症的项目中,证据等级最高、最有价值的生物标志物是PD-L1、TMB和MSI/MMR。
PD-L1
PD-1与PD-L1是一对对应的免疫检查点,其中PD-1位于免疫细胞(尤其是T细胞)表面,PD-L1位于各类体细胞表面。当T细胞PD-1与任何来源的PD-L1结合时,T细胞就会将该来源细胞视为“健康细胞”,对于该细胞的杀伤能力大幅度下降(下图左)。
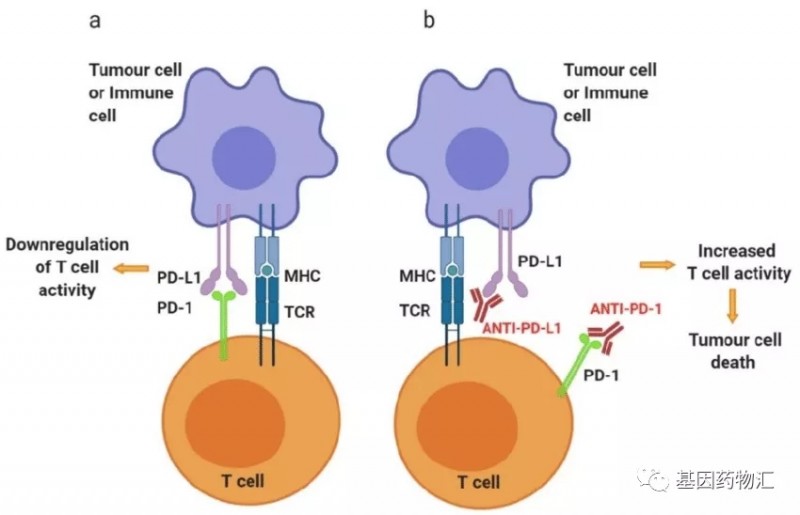
而PD-1/PD-L1抑制剂则是通过小分子物质,人为地将PD-1和PD-L1之间的结合阻断,从而避免癌细胞对于T细胞免疫功能的抑制(上图右)。
我们常说的PD-L1检测,通常情况下是检测患者癌细胞或肿瘤浸润淋巴细胞的PD-L1表达情况。当这两类细胞的PD-L1表达水平很高的时候,患者体内的T细胞在病灶区域内受到的抑制非常明显,解除这种抑制之后可能得到的免疫功能提升也更加显著。
目前,PD-L1检测的金标准是免疫组化检测。如果没有条件取得肿瘤组织,也可以通过其它基因检测来完成。
TMB
TMB的中文名称是肿瘤突变负荷,指肿瘤基因组编码区平均每百万碱基中被检测出的,体细胞基因编码错误、碱基替换、基因插入或缺失错误的总数。用于肿瘤患者时,TMB体现了患者癌细胞突变的总数。
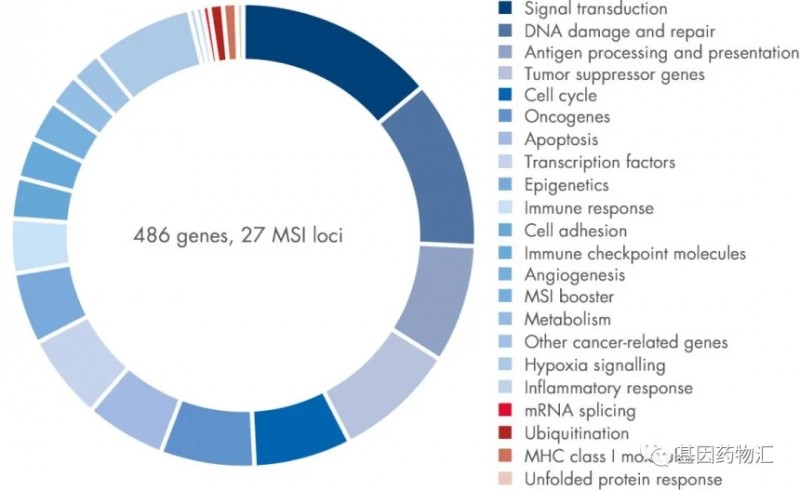
患者的肿瘤突变负荷越高,意味着癌细胞可能产生的新抗原越多,换句话说就是癌细胞和健康细胞的抗原标志物差距越大,因此免疫细胞就越容易识别和杀伤癌细胞,患者从免疫治疗中的获益也越大。
MSI/MMR
MMR指错配修复功能,其相关基因主要包括MLH1、MSH2、MSH6和PMS2等。这部分基因中的一个或多个的缺陷,会导致细胞无法发现和修改基因复制过程中出现的一些微小错误,进而造成广泛的MSI。
MSI的中文名称是微卫星不稳定性,MSI-H即微卫星不稳定性高,MSI-L即微卫星不稳定性低,与之相对的是MSS(微卫星稳定)。
所谓“微卫星”是一类很短的、具有重复单元的卫星DNA,又叫短串连重复或简单重复序列,类似于ATATATATATATATATATATATAT这种。在整个基因组中有超过10万个“微卫星”,目前已经查明的,与MSI-H直接相关的癌症包括结直肠癌(约15%)以及子宫内膜癌等。
发生MSI-H的比例较高的癌症类型还包括小肠肿瘤(约25%)、子宫内膜癌(约15%)、结直肠癌(约15%)和胃癌(约5%)等。
MSI-H和dMMR已经被确认为多款免疫药物应用的指标,这部分患者使用免疫治疗的疗效更好。
小汇有话说
而在MSI和TMB的关系方面,MSI-H的患者,大部分存在更高的TMB;但TMB高的原因并不只有MSI-H,有相当一部分患者MSS,但因为其它的原因而导致了TMB高。
换句话说,如果患者存在MSI-H,那么可以选择不做TMB的检测,因为97%的概率TMB也是高的;但如果患者TMB高,那么想要确定MSI还是MSS仍然需要再做相关的检测,只有16%的概率是MSI-H的。
这些类型的患者,用PD-1抑制剂的疗效更好
携带POLE/POLD1基因突变、CDK12基因缺失、PBRM1基因突变的患者,使用PD-1抑制剂,疗效较好。
POLE/POLD1
一项由中山大学徐瑞华教授团队完成、发布于顶级医学期刊《JAMAOncology》杂志上的研究中指出,携带POLE/POLD1基因突变的患者,使用PD-1抑制剂的疗效更好。
根据研究的结构,同样接受免疫治疗,存在POLE/POLD1基因突变的患者中位总生存期为34个月,不存在POLE/POLD1基因突变的患者仅有18个月。即使排除掉其中合并了MSI-H的患者,生存期的优势仍然非常显著(28个月vs16个月)。
CDK12
CDK12在维持细胞基因组的稳定方面有独特的作用。从机理上来说,CDK12的缺失可能导致DNA损伤修复基因表达沉默,造成细胞处于与损伤修复基因缺陷相同的状态。
部分试验已经证实了CDK12基因缺失的患者能够对PD-1抑制剂产生更好的响应。例如根据一项发布于2019年ESMO大会上的报告,CDK12基因缺失的前列腺癌患者,4~6线使用PD-1抑制剂治疗(包括派姆单抗及纳武单抗)的前列腺特异性抗原反应发生率为38%,中位无进展生存期6.6个月。
PBRM1/ARID2
一些研究认为,PBRM1/ARID2等基因突变的患者,对于免疫治疗的响应率更高。
这些类型的患者,不适合使用PD-1抑制剂
携带JAK1、JAK2、BM2、HLA、STK11等基因突变的患者,可能对PD-1抑制剂天然耐药。
驱动基因阳性的非小细胞肺癌患者,以及部分类型癌症的初治患者,不推荐使用PD-1抑制剂。
终末期、免疫功能衰败的患者,以及曾经发生过严重的自身免疫性疾病或免疫相关不良事件的患者,不推荐尝试PD-1抑制剂治疗。
这些类型的患者,谨慎用PD-1抑制剂
伴有MDM2/MDM4扩增、EGFR突变等的患者,使用PD-1/PD-L1抑制剂,可能发生爆发进展!
在一项派姆单抗(一种经典的PD-1抑制剂)的Ⅱ期临床试验中曾经招募过11例未接受过靶向治疗的EGFR突变型非小细胞肺癌患者,其中73%的患者PD-L1表达为强阳性(TPS≥50%)。
正常来说,这部分患者应该属于有很大希望对免疫治疗有良好响应的患者,但实际的疗效却是,仅有1例患者对派姆单抗的治疗有响应,缓解率仅9%;再次进行基因检测,研究者们惊讶地发现,这名患者的前一次检测结果错了,他其实根本没有EGFR突变!事实上,EGFR突变的患者接受派姆单抗治疗的响应率是0!
在这部分患者中,原本有64%属于EGFR抑制剂敏感性突变(包括EGFR19缺失和L858R突变),如果他们当初选择了靶向治疗,很可能会有完全不一样的治疗结局。这一方面凸显了基因检测对于免疫治疗结果预测的重要意义,一方面也说明了选对治疗方案对于患者的重要性。免疫治疗再好,也要用对适应症,否则一样毫无疗效。
除此以外,在研究进行的6个月内,已经有2例患者因严重的免疫相关不良事件死亡。EGFR突变患者接受PD-1/PD-L1抑制剂治疗,不仅疗效不尽如人意,副作用也更加严重。
很多其它临床试验也证实了这一点。奥希替尼联合得瓦鲁单抗(一种PD-L1抑制剂)治疗EGFR突变的非小细胞肺癌患者,不良反应中间质性肺病的发生率高达38%;吉非替尼联合得瓦鲁单抗治疗,3~4级肝酶升高的发生比例高达40%~70%。
一项meta研究综合分析了CheckMate057、KEYNOTE-010和POLAR共三项试验的结果,最终得到结论,在EGFR敏感突变阳性的患者中,使用PD-1/PD-L1抑制剂的疗效,甚至比不上使用多西他赛的疗效。
小汇有话说
“神药”虽“神”,但实际上也只是在其对应的适应症上“疗效如神”。许多患者和家属、甚至部分医生盲信“神药”的效果,不论病情如何统统使用PD-1抑制剂,其实很可能存在非常大的风险。
基因药物汇提醒大家,抗癌药物的应用必须谨慎,治疗方案的选择应当基于患者的独特病情。现如今,基因检测是详细了解患者疾病特点的重要手段,大家应该在完成了必要检测的基础之上,选择更合适的药物治疗方案。
如果大家需要药物的使用指导,申请新药临床试验或寻求更权威专家的会诊,可以联系全球肿瘤医生网医学部(),或将患者病历资料及联系方式发送至邮箱(doctorjona0404@gmail.com)。我们会安排专业顾问与您联系,帮助您解决困惑。
