胃癌靶向药物,2021年已上市的胃癌靶向治疗药物和胃癌免疫药物有哪些
胃癌是一种常见的恶性肿瘤,全球将近一半的新发胃癌患者和死亡病例在中国!胃癌的可怕之处在于,一旦发现,大部分患者已处于中晚期,治疗的方式非常有限,患者的生存面临着严峻的考验。
近年来,随着精准医学的兴起,胃癌的靶向和免疫治疗为患者带来了更多长生存希望!比如曲妥珠单抗在HER2阳性胃癌的治疗中有重要的意义,抗血管生成抑制剂的问世为许多无法接受手术的患者提供了治疗的可能,目前新兴的靶点Claudin18.2更是有望为超过半数的胃癌患者带来生机!众多新靶点药物的问世,为胃癌开启了一个全新的治疗模式,创造了新的可能性。
胃癌需要检测的基因靶点有哪些
胃癌虽然没有非小细胞肺癌或乳腺有那么多的驱动基因的改变,但也需要针对不同亚型,采取针对性的靶向疗法。
在2021年第一版胃癌的临床实践指南(NCCN)中明确指出胃癌应检测以下靶点:
01、新诊断胃癌:MSI/MMR纳入常规检测
与既往指南推荐转移性胃癌患者进行MSI/MMR检测不同,最新版指南建议,所有新诊断的患者都应进行MSI及MMR的检测。(研究证实,免疫检查点抑制剂治疗MSI-H/dMMR患者的效果明显好于传统的化疗或化疗联合靶向药物,因此对于MSI-H/dMMR患者,免疫检查点抑制剂也可作为早期胃癌患者新辅助治疗的选择。)
02、转移性胃癌
检测HER2,PD-L1。
03、NGS检测意义重大
除此之外,还有多种其它生物标志物成为靶向疗法的靶点,在临床试验中用于筛选胃癌患者。Claudin18.2、trop-2、c-MET、FGFR、NTRK、纤维生长因子等等受体,针对这些靶点的靶向疗法已经在临床试验中获得积极结果,有望进一步改善胃癌患者精准治疗的格局。因此NGS发现相关基因的变异就显得很有意义,基于此,最新版指南建议组织样本充足的患者进行NGS。
注:对于胃癌HER2检测,尽可能选择金标准检测方式(IHC/ISH),组织样本条件允许情况下再进行NGS。NGS液体活检,可用于无法进行组织活检的转移性或晚期胃癌患者。
胃癌突变靶点及获批药物解读
目前,针对胃癌的这些靶点共7种靶向及免疫药物已经获得批准上市。
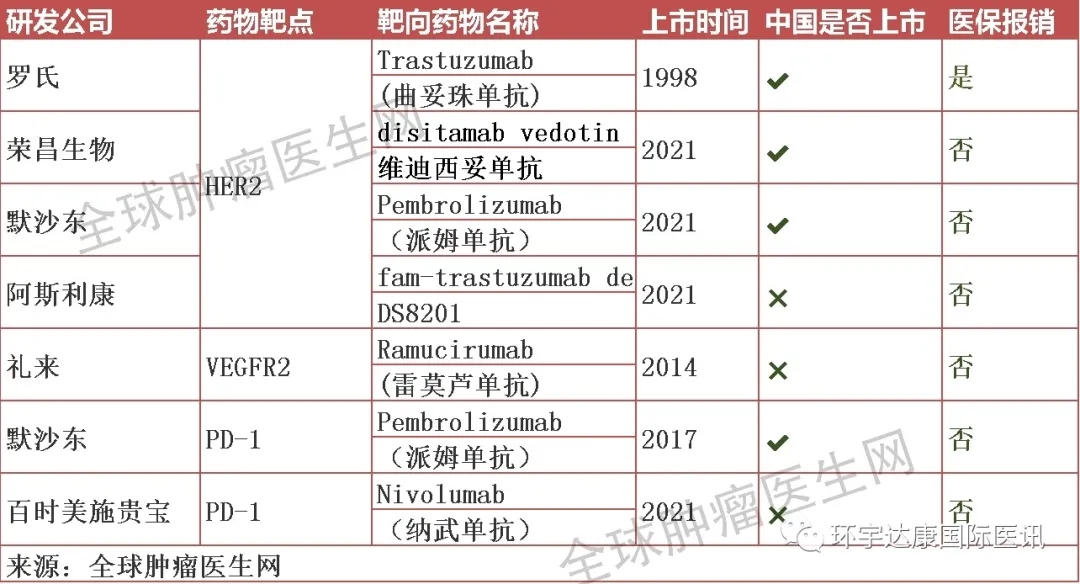
除了上面获批的药物,还有更多的新药正在研发中,包括ADC药物、MET抑制剂、PD-1/PD-L1抑制剂等等,大家可以根据当前疾病的发展情况以及分子分型进行选择,也可联系全球肿瘤医生网医学部()了解详细招募标准,进行入组评估。
01、HER2
第一个或者最重要的一个靶点,就是HER2这一个标志物。HER2在胃癌当中的表达率大概是在15%左右。目前晚期胃癌HER2治疗已获得全球共识,NCCN指南推荐胃癌患者检测HER2表达,如果检测结果显示HER2+,那么患者一线推荐使用曲妥珠单抗联合化疗。
1)曲妥珠单抗(Herceptin赫赛汀、Herzuma、Ogivri)
作用靶点:HER2
适应症:于HER2阳性转移性胃癌的一线治疗
药品详情:2012年10月,曲妥珠单抗批准可用于HER2阳性转移性胃癌的一线治疗(胃腺癌或胃食管连接处的腺癌)
2)fam-trastuzumabderuxtecan-nxki(Enhertu,DS-8201)
作用靶点:HER2
适应症:既往接受过基于曲妥珠单抗治疗的局部晚期或转移性HER2阳性胃或胃食管(GEJ)腺癌成人患者
药品详情:缓解率接近4倍!“生物导弹”已经上膛,DS-8201重拳出击!
Enhertu,也称DS-8201,是一款非常具有代表性的经典ADC药物。它主要由能够精准识别并靶向HER2的单克隆抗体,以及化疗药伊立替康组成。
2019年底,Enhertu已经获得FDA批准用于治疗HER2阳性乳腺癌;此后2020年9月,Enhertu又于日本获批了胃癌的适应症。2021年1月15日,FDA正式批准用于胃癌。
根据最新公开的研究结果,Enhertu治疗患者的中位总生存期为12.5个月,而接受化疗(伊立替康或紫杉醇)的患者中位总生存期为8.4个月。
在缓解率方面,接受Enhertu治疗的患者整体缓解率为40.5%,显著高于接受化疗患者的11.3%;接受Enhertu治疗患者的中位无进展生存期为5.6个月,中位缓解持续时间11.3个月,同样显著超过了化疗患者的3.5个月和3.9个月。
3)派姆单抗(keytruda,pembrolizumab)
作用靶点:HER2
适应症:联合曲妥珠单抗、氟嘧啶和含铂化疗药物用于局部晚期不可切除或转移性HER2阳性胃或胃食管交界处(GEJ)腺癌患者的一线治疗。
药品详情:超越曲妥珠单抗!派姆单抗联合方案获FDA批准,一线治疗胃癌缓解率74%!
2021年5月5日,美国食品药品监督管理局加速批准派姆单抗(Keytruda,MerckCo.)联合曲妥珠单抗、氟嘧啶和含铂化疗药物用于局部晚期不可切除或转移性HER2阳性胃或胃食管交界处(GEJ)腺癌患者的一线治疗。
4)维迪妥昔单抗(爱地希,disitamabvedotin,RC48,国内获批)
作用靶点:HER2
适应症:治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃及胃食管结合部腺癌患者
药品详情:获批了!首个国产药物-抗体偶联物(ADC)上市,“生物导弹”重装来袭!
2021年6月9日,我国荣昌生物自主研发的创新抗体-药物偶联物(ADC)维迪西妥单抗(RC48-C014)获得中国国家药品监督管理局批准上市,用于治疗至少接受过2种系统化疗的HER2过表达局部晚期或转移性胃及胃食管结合部腺癌患者。
这是我国获准上市的首款国产ADC药物,不仅代表着多线耐药的HER2阳性胃癌患者拥有了全新的后线、末线治疗选择,也标志着我国的癌症精准治疗进入了一个全新的时代。
02、VEGF
1)雷莫芦单抗(ramucirumab,Cyramza®)
作用靶点:VEGF
适应症:接受过氟嘧啶或含铂化疗后疾病进展的晚期胃或胃食管结合部腺癌患者的治疗。
药品详情:2014年4月21日,FDA批准雷莫芦单抗用于接受过氟嘧啶或含铂化疗后疾病进展的晚期胃或胃食管结合部腺癌患者的治疗。成为第一个化疗后进展晚期胃癌患者的治疗药物。
2)甲磺酸阿帕替尼(国内获批)
作用靶点:VEGF
适应症:晚期胃癌或胃食管结合部腺癌患者三线及三线以上治疗。
药品详情:
除了雷莫芦单抗,还有一款在国内上市的抗血管生成药物甲磺酸阿帕替尼,是我国自主研发新药,其主要作用机制是竞争性结合该受体胞内酪氨酸ATP结合位点,高度选择性地抑制VEGFR-2酪氨酸激酶活性,阻断VEGF通路信号转导,从而有效抑制肿瘤血管生成。中国国家药监局于2014年10月17日正式批准其用于晚期胃癌或胃食管结合部腺癌患者三线及三线以上治疗。
03、PD-1
1)nivolumab(Opdivo,纳武单抗)
作用靶点:PD-1
适应症:已接受新辅助放化疗的完全切除的食管或胃食管交界处(GEJ)癌残留病理患者
药品详情:2021年5月20日,美国食品药品监督管理局批准nivolumab(Opdivo,百时美施贵宝公司)用于已接受新辅助放化疗的完全切除的食管或胃食管交界处(GEJ)癌患者。
2021年4月16日,美国食品药品监督管理局批准nivolumab(Opdivo,百时美施贵宝公司)联合含氟嘧啶和含铂化疗药物治疗晚期或转移性胃癌、胃食管交界处癌和食管腺癌。
2020年3月,中国国家药品监督管理局正式批准欧狄沃(纳武利尤单抗注射液)用于治疗既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管交界腺癌患者。(PD-L1阳性)
这是中国首个也是目前唯一一个获批用于晚期胃癌的免疫治疗药物,也是迄今唯一经过Ⅲ期临床试验证实能为中国晚期胃癌患者带来生存获益的PD-1抑制剂。
2)派姆单抗(keytruda,pembrolizumab)
作用靶点:PD-1
适应症:联合铂类和氟嘧啶类化疗药物一线治疗转移性或局部晚期食管或胃食管(GEJ)癌,不适合手术切除或根治性放化疗。
药品详情:
2021年3月22日,美国食品药品监督管理局批准派姆单抗(Keytruda、默克夏普和多美公司)联合铂类和氟嘧啶类化疗药物用于转移性或局部晚期食管或胃食管(GEJ)癌,不适合手术切除或根治性放化疗。
2017年9月,FDA批准派姆单抗用于已经接受过至少2次治疗(包括化疗)的晚期胃癌患者,用于治疗复发性局部晚期或转移性胃或胃食管连接(GEJ)腺癌的患者,其肿瘤表达PD-L1[综合阳性评分(CPS)≥1],由FDA批准的测试确定。在包括含氟嘧啶和铂的化学疗法,或者HER2/neu靶向疗法两线或多线治疗后进展。另外,基因检测结果MSI-H的胃癌患者也适用。
未完待续!期待更多新药开花结果
除此之外,还有一些在研的新型靶向,免疫治疗药物在胃癌的治疗上取得了很好的疗效!随着新型临床研究如雨伞篮子研究的推进,对检测提出了更高要求,需要全面了解患者的基因图谱,已经做了检测的可以致电全球肿瘤医生网医学部全面的解读报告获得用药方案及临床试验推荐。相信胃癌患者的明天会越来越好。
下一期我们将为病友们系统整理肺癌各靶点的全球研发进展,想接受治疗的患者可以申请专家会诊评估用药方案或参加方舟计划获得免费用药的机会。让我们拭目以待,期待更多新药早日上市,造福大众!
“方舟援助计划”“由全球肿瘤医生网联合无癌家园、权威基因检测机构、国际药厂、知名肿瘤中心发起的针对癌症基因突变肿瘤患者的活动。本计划旨在降低肿瘤患者基因检测费用,为患者提供上市新药和未上市新药免费治疗的机会。参加“方舟援助计划”!为肿瘤患者持续提供抗癌药物带来的生存希望!
想参加的病友可以将基因检测报告,诊断报告电子版或拍照发送至doctor.huang@globecancer.com,邮件中留下联系方式,医学部收到报告分析完毕后一个工作日内电话联系或直接致电全球肿瘤医生网医学部评估。
国际知名胃癌专家

JeffreyMeyerhardt
丹娜法伯癌症研究院

MilindJavle
MD安德森癌症中心

KimmieNg
丹娜法伯癌症研究院

ThomasA.Abrams
丹娜法伯癌症研究院
