肺癌新药,新一代ROS1抑制剂瑞普替尼治疗肺癌疾病控制率高达94%
94%患者肿瘤控制稳定,显著缩小甚至消失!ROS1肺癌患者迎来疗效更佳的治疗选择。
中国每年有80多万新诊断的肺癌患者,其中非小细胞肺癌(NSCLC)占约85%,约2%-3%的晚期NSCLC患者存在ROS1融合,这些患者面临两大生存挑战:
首先,至少50%使用目前获批的克唑替尼和恩曲替尼后会出现耐药;
其次,ROS1融合阳性非小细胞肺癌患者中很容易出现脑转移,目前的两款药物的颅内活动并不理想。临床迫切需要更有效的治疗方案。
近日,全新一代ROS1抑制剂repotrectinib(瑞普替尼)公布了最新的1/2期代号为TRIDENT-1研究的数据,结果显示:Repotrectinib在ROS1融合阳性非小细胞肺癌患者中具有持久的临床活性,无论之前是否接受过ROS1靶向治疗。这项研究发表在国际顶级期刊《新英格兰医学杂志》上,引起巨大轰动。

94%患者获益!肺癌新药Repotrectinib为ROS1患者点亮希望
Repotrectinib——这款针对ROS1阳性晚期NSCLC的全球重磅新药一直被誉为“同类最佳药物”。
值得中国病友们振奋的是,在全球和中国的临床数据表明,无论是初治还是经治的晚期患者,瑞普替尼都显示出了积极的临床有效率,中国的患者与全球各地的临床研究中心的数据结果相近,有望进一步延长ROS1+非小细胞肺癌的生存期!
截至2022年12月19日,纳入汇总分析的352名ROS1融合阳性非小细胞肺癌患者接受了至少一剂瑞普替尼的治疗,招募期间大量中国大陆受试者通过全球肿瘤医生网成功入组接受治疗,结果非常振奋人心。
一:初治队列-94%患者获益
71名未接受ROS1TKI治疗的非小细胞肺癌患者,总客观缓解率(cORR)为79%,其中7名患者(10%)达到完全缓解(CR);49名患者(69%)达到部分缓解(PR)。疾病控制率高达94%!
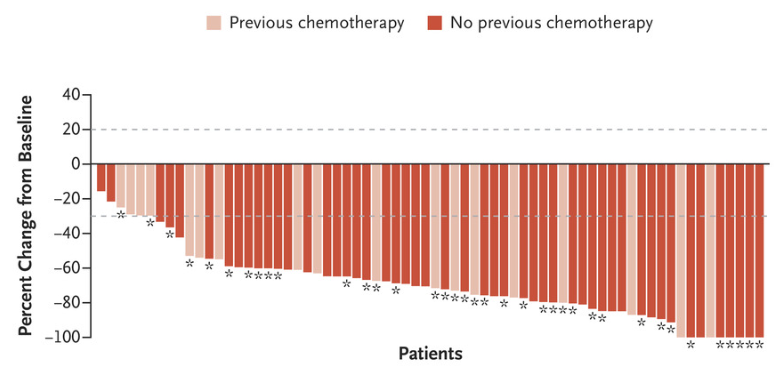
二:接受过一种ROS1抑制剂未接受化疗治疗的队列
56名接受过1种ROS1抑制剂治疗的非小细胞肺癌患者,总客观缓解率(cORR)为38%;其中3名患者(5%)获得完全缓解,18名患者(32%)获得部分缓解。
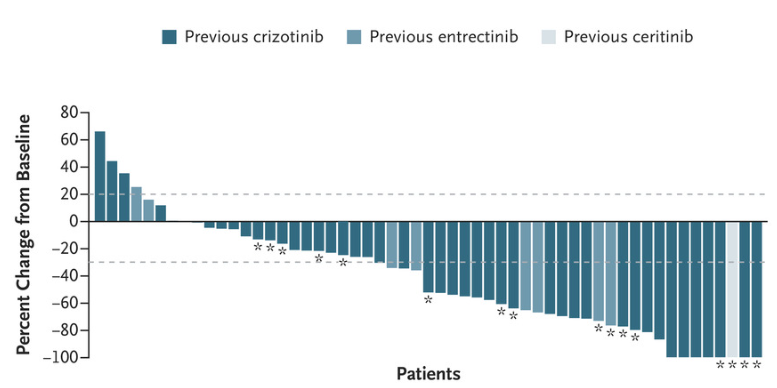
此外,这款药物具有强大的入脑活性。在基线时具有可测量脑转移的患者中,9名先前未接受过ROS1TKI治疗的患者中,有8名(89%)发生了颅内缓解;13名之前接受过一种ROS1TKI并且从未接受过化疗的患者中,5名(38%)患者发生了颅内缓解。
因此,Repotrectinib具有持久的活性,并在高比例的ROS1融合阳性NSCLC患者中产生缓解,其中包括先前未接受过ROS1TKI治疗的肿瘤患者、先前接受过ROS1TKI治疗的肿瘤、ROS1G2032R耐药突变和脑转移的患者。
全新一代抗癌药瑞普替尼已上市!国内多中心启动临床
相信看了上面的数据,ROS1肺癌患者一定重新燃起了希望!更好的消息是,2023年11月15日,FDA已正式批准repotrectinib(瑞普替尼)上市,用于治疗局部晚期或转移性ROS1阳性非小细胞肺癌成年患者。特别值得一提的是,这是全球首款获批上市的第二代NTRK/ROS1抑制剂,同时,这款药物也有了自己响当当的大名--Augtyro。
2023年5月18日,中国国家药品监督管理局(NMPA)药品审评中心(CDE)授予肺癌新药瑞普替尼(repotrectinib)优先审查资格,暨美国上市后,这款药物也即将在中国获批,造福患者!
更好的消息是,目前中国正式开展repotrectinib(TPX-0005)治疗ROS1突变晚期非小细胞肺癌和NTRK阳性晚期实体瘤的II期TRIDENT-1研究,已有大量中国大陆受试者通过全球肿瘤医生网抗癌新药招募中心成功入组接受治疗!
这意味着,我们国家终于和美国等医疗水平发达国家同步,加快抗癌“特药”的临床试验及上市审批!国内的患者也终于有机会免费接受这些天价“传奇”抗癌药物的治疗。
正在进行的1/2期TRIDENT-1研究招募初治的ROS1+晚期非小细胞肺癌患者。
注:做了基因检测报告的病友,快看看自己的报告是否存在ROS1或NTRK融合,一旦存在可以马上联系医学部看看是否有机会接受新药治疗,看不懂的病友也可以致电全球肿瘤医生网医学部解读报告。
申请流程
需要申请临床试验的患者需将基因检测报告、病理报告提交至全球肿瘤医生网医学部进行初步评估(照片发送至doctor.huang@globecancer.com,邮件中留下联系方式或直接致电医学部),我们的专家将为您全面分析解读检测报告,一个工作日内电话联系推荐新药及用药方案,并匹配适合入组的临床试验项目。
希望这项研究顺利进行,让这款抗癌新药能早日在中国获批上市,为更多患者带来获益!
除了瑞普替尼,AB-106、NVL-520、HG030等新一代药物,给ROS1融合及耐药的患者带来了全新的选择。众多国内病友已通过全球肿瘤医生网抗癌新药招募中心成功入组接受治疗!
需要提醒大家的是,即使是标准治疗方案失败,也可以尝试进行基因检测,一旦存在ROS1,NTRK1、NTRK2或者NTRK3基因融合,就可以尝试这些特效的广谱抗癌药。希望这款药物早日在国内获批上市,造福更多的患者!
参考资料:
https://www.nejm.org/doi/full/10.1056/NEJMoa2302299USFoodandDrugAdministrationapprovesAugtyro™(repotrectinib),anext-generationTyrosineKinaseInhibitor(TKI),forthetreatmentofLocallyadvancedormetastaticROS1-positivenon-smallcelllungcancer(NSCLC).Newsrelease.BristolMyersSquibb.November15,2023.AccessedNovember15,2023.
https://news.bms.com/news/corporate-financial/2023/U.S.-Food-and-Drug-Administration-Approves-Augtyro-repotrectinib-a-Next-Generation-Tyrosine-Kinase-Inhibitor-TKI-for-the-Treatment-of-Locally-Advanced-or-Metastatic-ROS1-Positive-Non-Small-Cell-Lung-Cancer-NSCLC/default.aspx
