EGFR20ins突变靶向药新药相继问世,EGFR20ins的肺癌患者迎来曙光
在肺癌中有一类特殊的亚型,即EGFR20ins突变,此类突变不仅治疗困难,而且新药研发进展缓慢。不过近年随着癌症研究的不断深入,这一罕见靶点逐渐被关注。自2021年5月21日,针对肺癌EGFR20ins突变的首款靶向药——Rybrevant获FDA批准上市以来,更多的靶向药相继问世。
截至2024年2月,中国、美国共批准4款可用于治疗EGFRex20ins突变非小细胞肺癌的靶向药物,另有多款在研药物效果惊艳值得期待,就此也正式开启了肺癌治疗的新纪元!下面全球肿瘤医生网小编帮大家做个简单汇总,以供参考!
肺癌中的难治性靶点:EGFR20ins
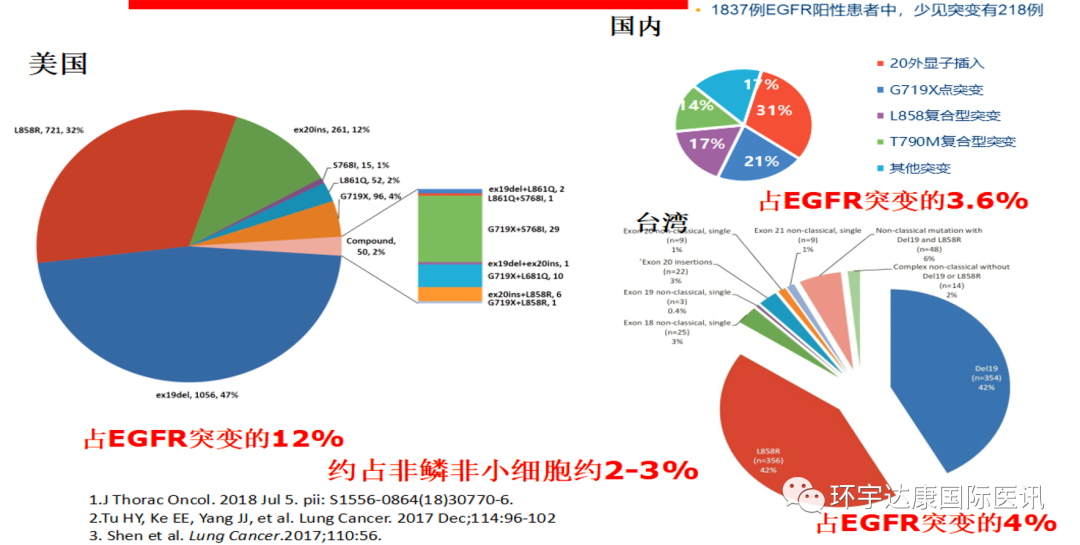
EGFR(表皮生长因子受体)突变是肺癌患者中最常见的靶点之一,我国约40%~50%的非小细胞肺癌(NSCLC)患者可见此类突变。在EGFR突变中,除了常见的Ex19de和L858R突变(约占90%)外,还有一列特殊的亚型——即EGFR外显子20插入突变(EGFRex20ins)。
EGFR20ins是一类分子异质性很强的变异类型,对一至三代EGFR酪氨酸激酶抑制剂(EGFR-TKIs)普遍原发耐药,而且对既往的化疗、免疫治疗等效果有限,预后较差。
不过好消息是,随着临床越来越多化合物的探索,针对这一罕见靶点的多款靶向药物先后获批上市,为EGFR20ins突变的肺癌患者带来了更多的生存希望!全球肿瘤医生小编为肺癌患者整理汇总了,目前已获批上市的靶向EGFR的肺癌药,详见下表:
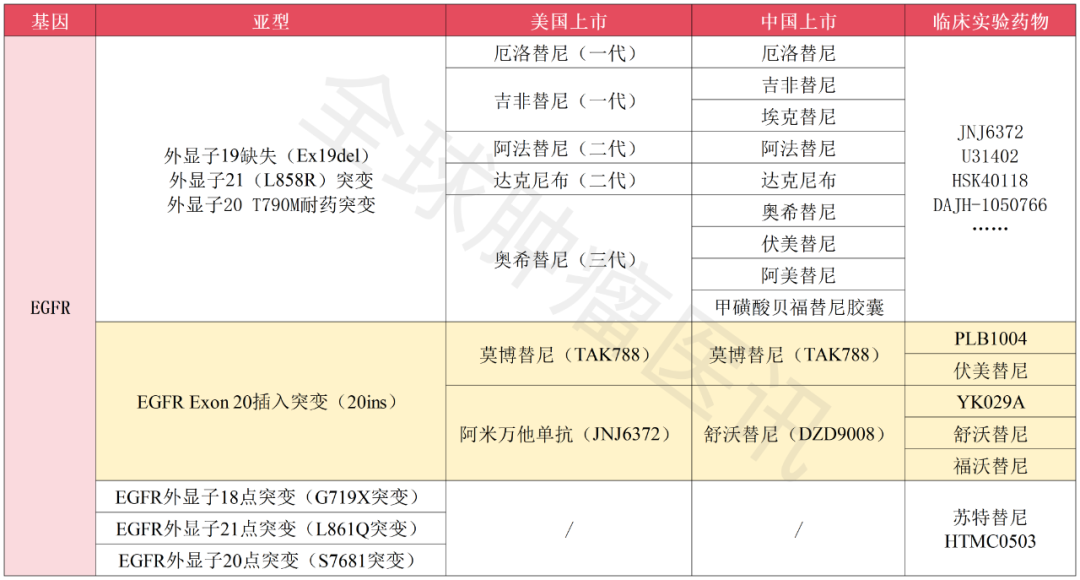
做了基因检测的病友可以拿出报告看看,一旦存在EGFR突变,可联系医学部,初步评估是否有机会接受国内新药治疗,看不懂的病友也可致电全球肿瘤医生网医学部解读报告。
中国获批药物
1、莫博赛替尼:中位OS为24个月
▲截图源自“NMPA官网”
2023年1月11日,琥珀酸莫博赛替尼胶囊(Mobocertinib,Exkivity,代号为TAK-788),获中国国家药品监督管理局(NMPA)批准,用于治疗EGFR20ins(EGFR外显子20插入)突变的非小细胞肺癌成年患者。
莫博赛替尼是一类口服的酪氨酸激酶抑制剂(TKI),专门设计用于针对EGFRExon20插入突变。这也是国内首款针对肺癌EGFR20ins突变的靶向疗法,具有里程碑式的意义!
莫博赛替尼本次在国内获批是基于1/2期临床试验(EXKIVITY)的积极结果。本次入组的114例EGFRExon20插入突变的非小细胞肺癌患者,既往接受过铂类治疗,入组后接受了莫博赛替尼治疗。结果如下:
整体缓解率(ORR):研究者评估Mobocertinib(莫博赛替尼)治疗的整体缓解率(ORR)为35%,独立评审委员会评估该药治疗的ORR为28%。
中位总生存期(OS):患者中位OS为24个月。
中位无进展生存期(PFS):患者中位PFS为7.3个月(95%CI:5.5~9.2),详见下图。
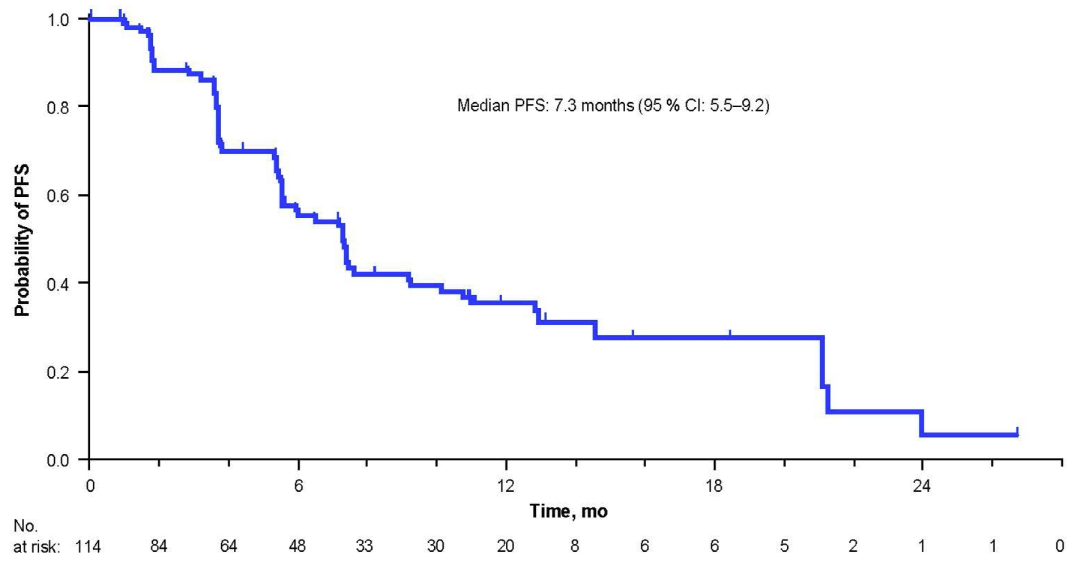
▲图源“JAMANetwork”
常见不良反应(20%):患者治疗后常见的不良反应包括恶心、呕吐、食欲下降、疲劳、口腔炎、皮疹、腹泻、皮肤干燥、甲沟炎、肌肉骨骼疼痛等。
2、舒沃替尼:近90%患者肿瘤缩小或稳定
2023年8月23日,舒沃替尼片(舒沃哲®,Sunvozertinib,DZD9008)获中国国家药品监督管理局正式批准上市,用于治疗EGFR外显子20插入(EGFR20ins)突变的非小细胞肺癌成年患者。舒沃替尼是由迪哲(江苏)医药公司研发的新型选择性、不可逆的EGFR/HER2抑制剂,无论突变位置如何,该药对约30种EGFR外显子20插入亚型,均具有抗肿瘤活性,旨在针对广泛的EGFR突变。它是中国首款上市的国研EGFR20ins突变的中国创新药物,在肺癌的治疗史上留下了浓墨重彩的一笔!
此次获批是基于舒沃替尼中国注册临床试验(WU-KONG6)的2期惊艳数据,其详细数据在2023年美国临床肿瘤学会(ASCO)上公布。本次共入组97例晚期EGFR20ins非小细胞肺癌难治性患者,这些患者既往都接受过1~4种全身治疗(包括抗VEGF治疗、靶向治疗、PD-1治疗)等,且在化疗后出现疾病进展。入组后给予舒沃替尼治疗,结果显示:
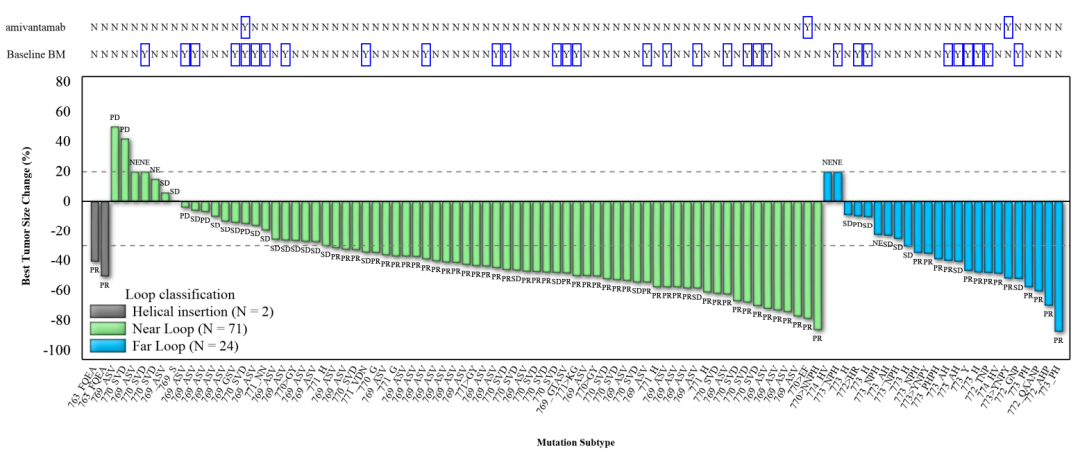
舒沃替尼在一次给药(300mg)时,达到了60.8%的总客观缓解率(ORR),和87.6%的疾病控制率(DCR)。这意味着近90%接受该药治疗的患者,其肿瘤不同程度的缩小或稳定。并且在基线时或接受埃万妥单抗(amivantamab)治疗后有脑转移的患者,也出现肿瘤缩小的表现。
更值得一提的是,在螺旋插入患者(n=2)的ORR高达100%,DCR为100%,近环分类患者(n=71)的ORR为62.0%,DCR为88.7%。在远环分类(n=24)组中,ORR为54.2%,DCR为83.3%(详见下图)。
美国获批药物
1、Rybrevant:首款EGFR20ins靶向药

2021年5月21日,Rybrevant(阿米万他单抗,amivantamab-vmjw,代号为JNJ6372),获FDA正式批准上市,该药是一种针对EGFR及MET受体的全人双特异性抗体,可抑制肿瘤生长并导致肿瘤细胞死亡,用于治疗在含铂化疗期间或之后,病情恶化的局部晚期或转移性EGFR外显子20插入突变(20ins)的非小细胞肺癌成年患者。Rybrevant是首款上市的肺癌EGFR20ins靶向疗法,这也意味着具有EGFR20ins突变的非小细胞肺癌患者,将首次获得靶向治疗的选择权,具有划时代的意义!
在一项“将Rybrevant作为单一疗法,治疗晚期非小细胞肺癌(NSCLC)”的I/Ib期EDI1001(CHRYSALIS)临床研究,共纳入153例具有EGFR外显子20插入(EGFR20ins)突变的患者,中位年龄为61.0岁,大多数患者被诊断为IV期腺癌(78.9%),且病情在铂类化疗期间或之后出现进展。截至2021年3月30日,经过为期14.5个月的中位随访,结果显示:
1.客观缓解率(ORR):在主要疗效人群(N=81)里,共有31名患者(38.3%;95%CI,27.7%to49.7%)达到了每位研究者评估的ORR,35名患者(43.2%;95%CI,32.2%to49.7%)达到了ORR。此外,根据研究者评估,对治疗的最佳反应仅包括部分反应(PR)(31名;38.3%)。
2.中位总生存期(OS):中位OS预估为22.77个月(95%CI,17.48至不可估计)。6个月时预估生存率为90%(95%CI,81%至95%),12个月时生存率为74%(95%CI,63%至83%)、41%(95%CI,21%至95%)。
图1每个研究者评估的总生存期(OS)的Kaplan-Meier图
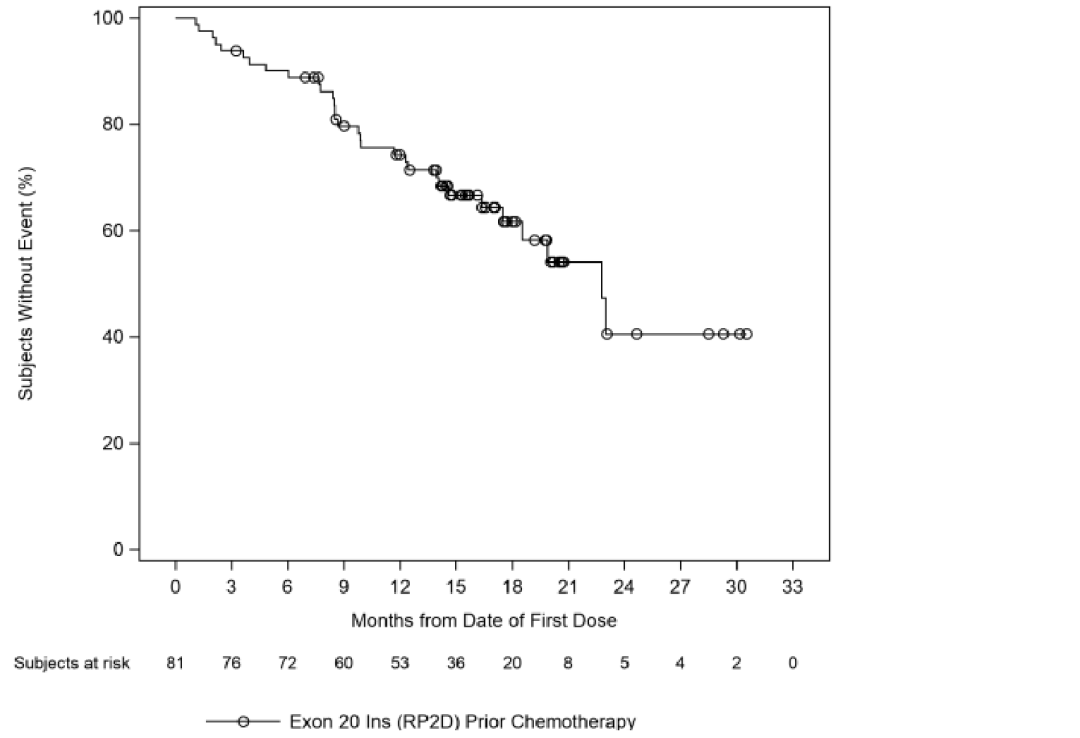
▲图源“CHRYSALISCSR中期分析”(2021年3月30日)
3.中位无进展生存期(PFS):患者的中位PFS为8.25个月(95%CI,5.49至12.32)。根据研究者评估,Rybrevant的无进展率在3个月时为75%(95%CI,64%至83%),在6个月时为58%(95%CI,47%至68%),在6个月时为40%(95%CI)(详见下图)。
图2PFS的Kaplan–Meier生存曲线图
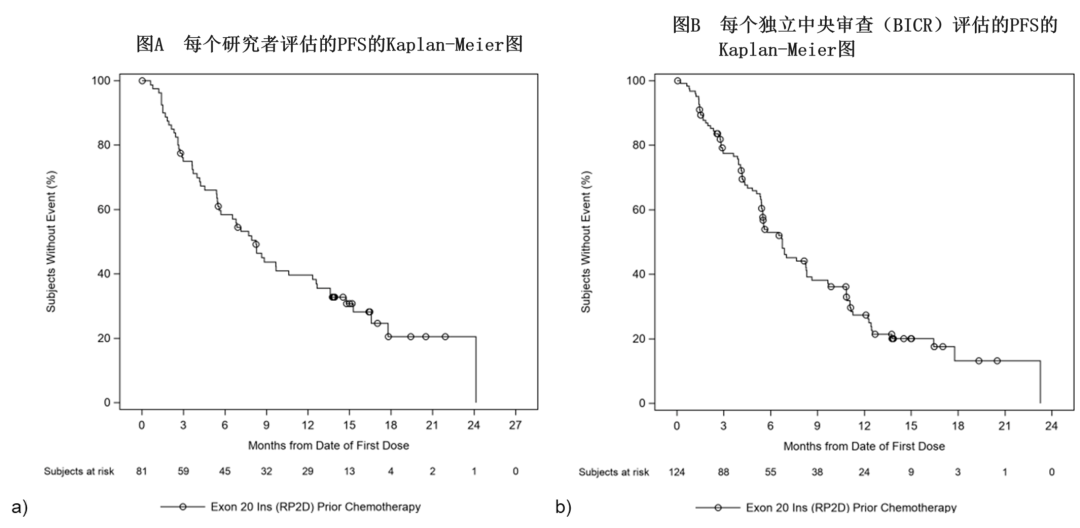
▲图源“CHRYSALISCSR中期分析”(2021年3月30日)
4.中位缓解持续时间(DOR):在31名缓解者中,中位治疗持续时间为14.03个月,中位DOR为12.45个月(95%CI,6.54至16.13)。
5.不良事件(TEAE):治疗后常见的不良反应包括输液相关反应(IRR)、甲沟炎、口腔炎、皮疹、痤疮样皮炎、低蛋白血症等。
2、莫博替尼:肺癌EGFR20ins第二款靶向药

2021年9月16日,Exkivity(mobocertinib,莫博替尼,代号为TAK-788)获FDA正是批准上市,该药为一种口服的氨酸激酶抑制剂(TKI),这是EGFR外显子20插入突变(EGFR20ins)肺癌患者的第二款靶向疗法,也是首款获批的专门针对EGFR20ins突变设计的口服疗法,具有重要的历史意义!
中国在2023年1月获批的琥珀酸莫博赛替尼胶囊,代号正是TAK-788,也是用于治疗EGFR20ins突变的非小细胞肺癌。
希望之光!EGFR20ins众多新药招募进行时
除了已经获批的几款药物外,针对EGFR20号外显子插入突变(EGFR20ins)这一罕见突变类型,目前还有多款临床新药研发项目正在火热进行中,为曾经无药可治的患者带来了新的希望!下面全球肿瘤医生网小编帮大家汇总了几款突破性新药,以供参考!
1、伏美替尼
药物名称:伏美替尼(AST2818,艾弗沙)。
研发公司:艾力斯。
作用靶点:EGFR20ins。
适应证:二线治疗EGFR突变20ins阳性肺癌。
药物介绍:伏美替尼是我国自主研发的第三代EGFR靶向药,在2021年欧洲肿瘤内科学会(ESMO)年会上公布的研究结果显示,该药治疗EGFR20外显子插入突变(EGFR20ins)晚期非小细胞肺癌(NSCLC)的效果惊艳,所有入组患者均出现靶病灶肿瘤缩小,肿瘤平均缩小约51.8%,疾病控制率高达100%!
招募信息:伏美替尼治疗EGFR20ins非小细胞肺癌的初Ib期临床研究项目已在国内启动,目前正在招募患者。
2、PLB-1004
药物名称:PLB1004。
研发公司:北京鞍石生物科技有限公司。
作用靶点:EGFR20ins。
适应证:二线治疗EGFR突变肺癌。
药物介绍:PLB-1004是我国自主研发的、拥有全球知识产权的新型单苯胺基嘧啶小分子EGFR抑制剂,同时也是第三代EGFR靶向药,于2020年2月获国家药品监督管理局(NMPA)临床试验默示许可,拟用于治疗非小细胞肺癌。该药不仅能有效且不可逆地靶向外显子20插入突变(20ins),同时还可针对经典EGFR突变ExDel19、T790M、L858R。目前PLB-1004在“治疗EGFR20ins非小细胞肺癌”的首次人体剂量递增和扩展的中期研究结果惊艳,不仅具有良好的疗效和安全性,同时有超过60%的肺癌脑转移患者获益。
招募信息(部分):目前正在招募组织学或细胞学证实的局部晚期或转移性(IIIB/IIIC/IV期)EGFR20ins突变型NSCLC患者;且既往接受标准治疗后疾病进展。
3、JMT-101
药物名称:JMT-101。
研发公司:津曼特。
作用靶点:EGFR20ins。
适应证:二线治疗EGFR突变20ins阳性肺癌。
药物介绍:JMT101为人源化抗EGFR单克隆抗体,具有自主知识产权,相较于国内外已上市的同类产品(如帕尼单抗、西妥昔单抗等),具有药效更优、免疫原性更低、亲和力更高的优势。该产品于2016年5月获得CFDA临床批件,现已进入I期临床研究,拟用于治疗非小细胞肺癌、结直肠癌等多款实体瘤。
招募信息(部分):目前正在招募ⅢB或Ⅳ期非小细胞肺癌,不适合进行根治性手术或放疗,且证实具有EGFR20号外显子插入(EGFR20ins)突变(包括重复突变),至少接受过含铂化疗的EGFRex20ins非小细胞肺癌,允许联合贝伐珠单抗或免疫检查点抑制剂;并排除EGFR抑制剂用药史。
4、HSK40118片
药物名称:HSK40118。
研发公司:海思科。
作用靶点:EGFR、EGFR20ins、EGFRC797S。
适应证:EGFR突变阳性肺癌。
药物介绍:HSK40118是一款口服的EGFR-PROTAC小分子抗肿瘤药物,也是第四代靶向药,有望延缓甚至克服因长期使用EGFRTKI导致的EGFR耐药突变问题。
招募信息:评估HSK401118在EGFR突变的晚期非小细胞肺癌患者中的有效性、安全性及耐受性的I期临床研究,纳入标准为携带EGFR突变且既往至少接受过一种EGFR-TKI治疗后,疾病进展的晚期非小细胞肺癌患者。
5、YK-029A片
药物名称:YK-029A。
研发公司:海南越康生物医药有限公司(为苏州浦合医药公司下属子公司)。
作用靶点:EGFR、EGFR20ins。
适应证:EGFRex20ins的晚期非小细胞肺癌(NSCLC)。
药物介绍:YK-029A是一种口服的、不可逆的第三代国研EGFR-TKI药物,为奥希替尼类似药。该药于2022年9月,纳入突破性治疗药物,适用于未经系统治疗的EGFR20外显子插入突变(EGFRex20ins)晚期非小细胞肺癌患者。“YK-029A一线治疗EGFRExon20ins肺癌”的Ⅰ期临床研究(CTR20180350)数据,在2022年CSCO年会上公布,结果显示,YK-029A治疗后的客观缓解率(ORR)达68.4%,疾病控制率(DCR)更是高达94.7%!
招募信息:评估对比含铂双药化疗,YK-029A片一线治疗EGFR20号外显子插入突变(EGFR20ins)的局部晚期或转移性非小细胞肺癌患者的Ⅲ期临床研究,纳入标准为携带EGFR20ins的初治肺癌患者,除外已知的合并ALK融合阳性或ROS1融合阳性或EGFR其他突变的患者。
6、BEBT-109
药物名称:BEBT-109。
研发公司:广州必贝特医药股份有限公司。
作用靶点:EGFR、EGFR20ins。
适应证:EGFR20号外显子插入突变(EGFR20ins)的局部晚期或转移性非小细胞肺癌。
药物介绍:BEBT-109是我国自主研发的一款高活性的泛突变型EGFR抑制剂,适用于EGFR突变阳性的非小细胞肺癌患者。临床前及临床研究显示,该药不仅对EGFR常见突变和T790M耐药突变具有高抑制活性,还对EGFR20号外显子插入突变(EGFR20ins)等稀有突变具有高抑制活性,目前已处于II期临床试验阶段。
招募信息:评估BEBT-109在“治疗EGFR20外显子插入突变(EGFR20ins),治疗局部晚期或转移性非小细胞肺癌的有效性、安全性”的II期临床研究,纳入标准为携带EGFR20ins的经治肺癌患者。
7、BAY2927088
药物名称:BAY2927088。
研发公司:拜耳医药保健有限公司(Bayer)。
作用靶点:EGFR20ins、EGFRC797S、HER2。
适应证:经治(一次全身化治疗后进展)的Her2、20ins阳性患者。
药物介绍:BAY2927088是一种选择性的二氢乳清酸脱氢酶(DHODH)抑制剂,可用于晚期非小细胞肺癌(NSCLC)、骨髓恶性肿瘤的相关研究。DHODH是一种在细胞分裂和DNA合成中发挥关键作用的酶,通过抑制该酶,可阻止癌细胞的分裂和增殖,达到抗癌的目的。
招募信息:评估BAY2927088在携带EGFR和/或HER2突变的晚期非小细胞肺癌(NSCLC)中的临床研究。纳入标准为经组织学或细胞学证实的局部晚期或复发转移性NSCLC,且既往接受过至少一种全身疗法治疗后,出现疾病进展。
小编寄语
在过去的十年间,肺癌的靶向免疫治疗已取得了长足的进展,我国的新药研发水平也已逐步进入世界前列!新药的快速研发,也为肺癌患者带来了新的曙光。我们也希望未来会有更多的新靶点、更多的新药物获批上市,让越来越多的罕见靶点患者有法可治、有药可医!
不过全球肿瘤医生网小编温馨提示,肿瘤患者在确诊后,不要病急乱投医,不可盲目相信民间偏方或保健品,积极寻找权威的肿瘤专家或医疗机构,仔细评估自身病情后,遵医嘱进行相应治疗,才是更为明智的选择!
如果您对目前的治疗有疑问,想要咨询专家会诊评估用药方案,或想参加方舟计划获得免费用药的机会,可咨询医学部,进行初步评估!
参考资料
[1]ZhouC,etal.TreatmentOutcomesandSafetyofMobocertinibinPlatinum-PretreatedPatientsWithEGFRExon20Insertion-PositiveMetastaticNon-SmallCellLungCancer:APhase1/2Open-labelNonrandomizedClinicalTrial.JAMAOncol.2021Dec1;7(12):e214761.
https://pubmed.ncbi.nlm.nih.gov/34647988/
[2]https://www.nmpa.gov.cn/index.html
[3]https://canjhealthtechnol.ca/index.php/cjht/article/view/PC0289r/1369
[4]https://aacrjournals.org/cancerres/article/83/8_Supplement/CT102/725358/Abstract-CT102-Interim-results-of-a-first-in-human
