ROS1属于酪氨酸激酶胰岛素受体的家族成员之一,在多种肿瘤细胞系中高表达,最初1987年在神经胶质细胞瘤中被发现。2007年Rikova等利用磷酸化蛋白质组学技术证实ROS1重排是非小细胞肺癌发生、发展中的驱动基因。随后证实克唑替尼和恩曲替尼对ROS1重排有效,并被批准用于临床治疗。日前,《自然评论临床肿瘤学》(NatureReviewsClinicalOncology)发表一篇对于肿瘤ROS1的综述文章,系统阐述了ROS1生物学功能、诊断方法、临床治疗策略及耐药机制[1]。
一ROS1生物学功能
ROS1基因位于第6号染色体q21区,全长cDNA包含44个外显子,编码2347个氨基酸,胰岛素受体的成员RTKs家族ROIS1与ALK,77%的的酪氨酸激酶结构域之间存在同源性,因此ALK小分子抑制剂克唑替尼在治疗ROS1发生融合变异的NSCLC中具有明显疗效。
在致病机理方面,尽管缺乏ROS1激活的合适配体或小分子激活剂,先前应用点突变和EGFR胞外受体部分构建的EGFR-ROS1嵌合蛋白表达技术业已证明,ROS1受体酪氨酸激酶参与激活多条下游信号转导通路,包括RAS-RAF-MEK-ERK,PI3K-AKT-mTOR和JAK-STAT3等通路,与肿瘤细胞增殖、存活和转移有关。
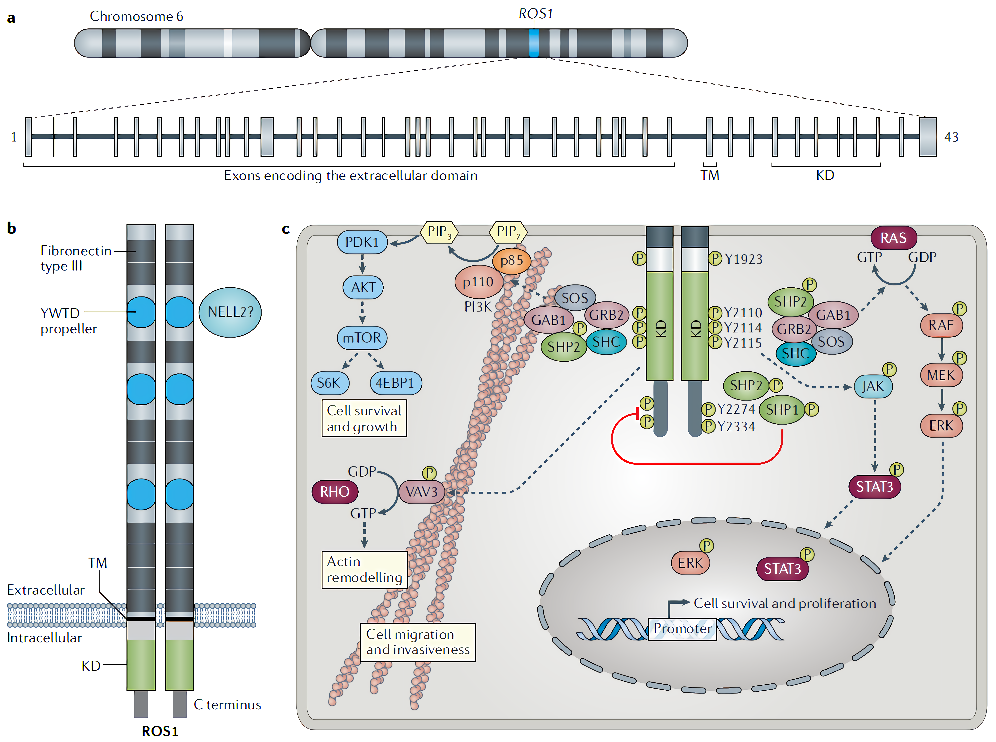
图1.ROS1基因结构和信号通路
二ROS1基因变异类型及分子诊断
ROS1基因变异包括融合、突变和扩增,融合是ROS1主要变异类型,目前至少发现55种伴侣基因。不同肿瘤,伴侣基因存在差异,NSCLC和神经胶质瘤主要伴侣基因分别为CD74和GOPC。已在22种肿瘤中检测到ROS1融合基因,不同肿瘤中ROS1融合基因发生率不同,NSCLC为1-2%,胃肠道肿瘤为1-9%,神经胶质瘤为0.5-1%。
目前检测ROS1融合基因的方法,包括传统的FISH、IHC、RT-PCR,但是这些方法存在一定的局限性,如灵敏度和特异性不够、无法得到融合断点及伴伴侣基因和只能检测已知融合形式等。随着NGS技术的发展,基于DNA-NGS或RNA-NGS的融合检测逐渐应用于临床,成为最优的融合检测方法。

图2.ROS1融合基因结构及细胞定位
三ROS1靶向治疗
目前,ROS1融合基因阳性的NSCLC患者,一线治疗NMPA和FDA批准了克唑替尼,同时FDA也批准了恩曲替尼,NCCN推荐色瑞替尼;在二线治疗中,NCCN推荐劳拉替尼[2]。已开展多种ROS1-TKI药物临床试验,克唑替尼治疗NSCLC的ORR最高达72%,中位PFS最高达22.8个月,颅内ORR达33%;恩曲替尼ORR、中位PFS和颅内ORR分别为77%、19.0个月和55%,恩曲替尼的颅内疗效优于克唑替尼。新型ROS1抑制剂劳拉替尼和Repotrectinib的ORR和颅内ORR数据表现很优秀,ORR分别为62%和91%,颅内ORR分别为64%和100%。
ROS1-TKI在其他肿瘤中的应用也有病例报告,如报道过克唑替尼治疗非典型脑膜瘤和肺母细胞瘤,色瑞替尼治疗乳腺癌和炎性肌纤维母细胞瘤的研究。此外有回顾性研究显示,克唑替尼治疗非CD74-ROS1的PFS长于CD74-ROS1,NSCLC脑转移患者的CD74-ROS1阳性率高于非CD74-ROS1,暗示融合基因的亚型可能影响肿瘤的颅内转移。
表1.ROS1-TKI在NSClC患者中的临床研究汇总
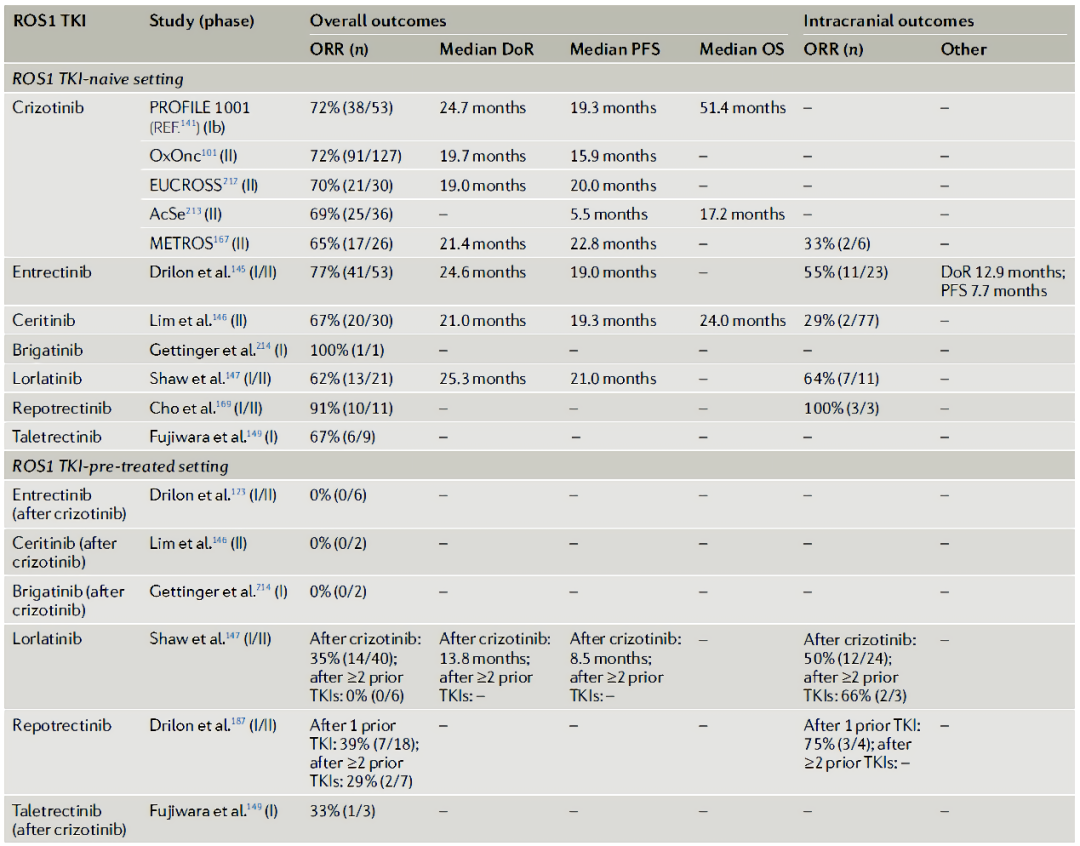

图3.ROS1-TKI在NSClC患者中的临床研究
四ROS1-TKI耐药机制
如果是ROS1融合基因阳性的NSCLC,可以使用靶向药物如克唑替尼进行相应的治疗。但往往治疗一段时间后,肿瘤会演变出新的耐药机制,耐药机制包括ROS1激酶区的突变和旁路激活。
ROS1激酶区的突变
如图4所示,在临床研究队列A和B中,耐药突变为8%和53%,而临床前研究的耐药突变比例远高于临床研究的,这些突变在晶体研究中也观察到。克唑替尼常见耐药突变为E1935G、L1947R、L1951R、G1971E、、L1982F、S1986F/Y、L2026M、G2032R、D2033N、C2060G、V2098I和L2155S;色瑞替尼耐药突变为E1990G和F1994L;恩曲替尼耐药突变为F2004C/I和G2032R。
旁路激活
旁路激活主要为RTK或MAPK信号通路基因突变或拷贝数增加,相关的基因有KRAS、NRAS、EGFR、HER2、MET、KIT、BRAF和MEK等。在临床治疗中,克唑替尼耐药出现KRASG12D和BRAFV600E突变,恩曲替尼出现NRASQ61K突变,另外ROS1-TKI治疗后还会出现CTNNB1S45F和PIK3CA热点突变。
目前对于肿瘤内和肿瘤间的ROS1-TKI耐药模式研究尚不充分,有研究报道一个病例,在cfDNA中检测到ROS1G2032R,而肺部肿瘤组织未检测到,用克唑替尼联合化疗治疗有效,但最终还是疾病进展,进展后在胸腔积液中也检测到ROS1G2032R。

图4.ROS1-TKI耐药机制
五小结
目前,在ROS1融合基因阳性NSCLC治疗上,克唑替尼和恩曲替尼获得上市批准,色瑞替尼和劳拉替尼获得NCCN指南推荐,新型ROS1-TKI正在开发中,将进一步提供更多临床切实有效的药物选择,今后对于临床ROS1融合基因阳性患者,也将有更多临床治疗选择。
参考文献
1.AlexanderDrilon,ChelseaJenkins,SudarshanIyer,etal.ROS1-dependentcancers-biology,diagnosticsandtherapeutics.NatureReviewsClinicalOncology(2020).
2.NCCNGuidelinesVersion2.2020Non-SmallCellLungCancer.